Лапароскопическая резекция желудка.
![]() Размещение
больного, операционной бригады, и оборудования.
Размещение
больного, операционной бригады, и оборудования.
![]() Техника.
Техника.
в. формирование окна в мезеколон;
д. формирование гастроэнтероанастомоза.
ЛАПАРОСКОПИЧЕСКАЯ РЕЗЕКЦИЯ ЖЕЛУДКА
Резекция желудка в хирургическом лечении язвенной болезни и рака желудка применяется уже более 100 лет и является одним из наиболее распространенных вмешательств современной хирургии. Не анализируя многочисленные дискуссии относительно оптимального выбора метода и техники резекции желудка, объемов ее, видов анастомозов и пр., укажем лишь на то, что резекция желудка является одним из основных инвалидизирующих факторов в хирургии, так как большая часть больных, перенесших эту операцию, возвращается к труду только спустя 4 - 6 месяцев после операции. Таким образом, восстановление трудоспособности больных после резекции желудка, снижение сроков временной нетрудоспособности являются насущной задачей клинической медицины.
Одним из очень весомых факторов снижения травматичности вмешательства является лапароскопический доступ с применением аппаратной технологии резекции желудка и наложения анастомоза, ч то, в свою очередь, приведет к существенному улучшению функциональных результатов, уменьшению послеоперационного пребывания больного в стационаре и общей нетрудоспособности.
Истории лапароскопических резекционных методов операций на желудке предшествовал этап гастростомии и различных вмешательств через гастростому, основателем которой в 60 - 70 гг. был российский хирург И. Д. Прудков.
Первые сообщения о лапароскопической резекции желудка появились в 1992 г. (Р. Goh с соавт., 1992, 1993; J. Lukaszczyk с соавт., 1992) и касались сегментарных резекций но поводу доброкачественных опухолей и язвы желудка, а затем и резекции желудка по Бильрот - 2 с наложением гастроэнтероанастомоза.
Строго говоря, передняя линейная резекция желудка, примененная для лечения язвенной болезни, в сочетании с задней стволовой ваготомией (Р. Gomez-Ferrer с соавт., 1992; А. С. Балалыкин с соавт., 1993) является прототипом лапароскопической желудочной хирургии.
Лапароскопичсские резекции желудка стали возможными благодаря хорошо разработанной и доведенной до стандартной технике наложения желудочно-кишечных анастомозов в различных вариантах (А. Cushieri 1994; Р. Lointier 1994). Материалы отдельных авторов в 1992 - 93 гг. насчитывали уже десятки резекций желудка и гастроэктомий, а, по данным интернационального клуба желудочной хирургии, в 1994 г. 18 хирургов из 13 стран накопили опыт 117 операций.
В России о первых операциях резекции желудка сообщили О. Э. Луцевич (1994) и В. П. Сажин с соавт. (1994), известно о проведенных операциях в клиниках С. И. Емельянова и В. И. Оноприева.
В открытой абдоминальной хирургии ныне совершенно определенно сформулированы показания для резекции желудка при язвенной болезни желудка. Избегая подробного освещения известных и устоявшихся положений, следует показания для резекции желудка в открытой хирургии сформулировать следующим образом:
1) длительно не заживающая, не поддающаяся комплексному медикаментозному лечению, рецидивирующая язва желудка,
2) подозрение на озлокачествление язвы,
3) опухоль желудка.
Проанализировав особенности технического выполнения лапароскопических резекций желудка по собственным наблюдениям, можно так сформулировать местные показания для выполнения этой операции:
1. наличие язвы желудка независимо от ее размеров;
2. отсутствие пенетрации язвы желудка в окружающие органы;
3. отсутствие прорастания и метастазирования опухоли желудка.
Наибольшие размеры, по нашим наблюдениям, достигали 3,5 см, при наличии язвенного инфильтрата - до 5 см. Большое значение для дифференцированного применения лапаросконической резекции желудка имеет степень подвижности желудка вместе с язвой. Этот фактор часто зависит от зоны перифокального воспаления и пенетрации язвы. Причем, если язва прорастает в брюшину, покрывающую поджелудочную железу или в поперечпо-желудочную связку, это не несет каких-либо осложнений и легко технически устранимо.
Общие противопоказания для выполнения лапароскопических операций на желудке:
1) ожирение II - III степени;
2) предшествующие операции на верхнем этаже брюшной полости;
3) признаки легочно-сердечной недостаточности;
4) заболевания крови;
5) беременность в поздних сроках.
При эндоскопических операциях на желудке обычно используются стандартный телехирургический комплекс. Следует обратить внимание на то, что целесообразно пользоваться инсуфляторами большой мощности (до 16 л/мин) и видеокамерой с хорошей разрешающей способностью (так называемые 3-чиповые камеры). Базовый инструмент должен включать троакары 12 - 15 мм в диаметре для введения сшивающих аппаратов, атравматические зажимы эндобэбкокк, автоматический клипаппликатор для наложения большого количества клипов (на одну операцию необходимо, как минимум, 2 инструмента, содержащих до 40 клипов), 3 - 5-лопастной ретрактор для отведения печени и других органов, для пересечения кишки и желудка, наложения анастомозов необходимы сшивающие аппараты с кассетами 30 и 60 мм, герниостеплер, рассасывающийся эндоскопический шовный материал, аппарат Endo-Stich для автоматического ручного шва. Обязательно использование двух мониторов.
Размещение больного, операционной бригады и оборудования
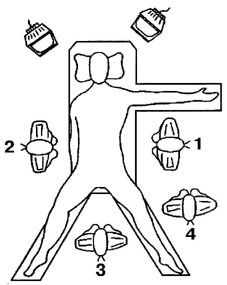 Рис.
1. Расположение операционной бригады при лапароскопической резекции желудка:
1) хирург; 2) ассистент; 3) оператор; 4) сестра.
Рис.
1. Расположение операционной бригады при лапароскопической резекции желудка:
1) хирург; 2) ассистент; 3) оператор; 4) сестра.
Положение больного при лапароскопической резекции желудка определяется техническими особенностями операционного стола, а также характером и количеством мониторов. На рис. 1 представлена позиция больного, наиболее удобная для выполнения лапароскопической резекции желудка. При расположении членов операционной бригады, независимо от количества мониторов, оперирующий хирург должен располагаться напротив оперируемого органа и напротив монитора. Благодаря такому расположению удается избежать "зеркально отраженного" манипулирования инструментами.
 Рис.
2. Операционные доступы при лапароскопической
резекции желудка.
Рис.
2. Операционные доступы при лапароскопической
резекции желудка.
Положение троакаров при лапароскопической резекции желудка может изменяться в зависимости от встречающихся по ходу операции анатомических особенностей верхнего этажа брюшной полости. На рис. 2 представлены точки введения троакаров. В точку 1, расположенную на 2 - 4 см выше пупка, по средней линии вводится 10-мм троакар для лапароскопа. Следующие точки 2, 3, 4, 5 предназначены для введения 12-мм троакаров. По ходу операции лапароскоп может перемещаться из точки 1 в точки 3, 4, 5. Необходимость перемещения лапароскопа в эти точки возникает при мобилизации желудка, формировании окна в мезоколон, при наложении гастроэнтероанастомоза. Точки 6 и 7 являются дополнительными и удобны при манипуляциях на верхнем отделе желудка (точка 6) или па большой кривизне и дне желудка (точка 7).
Исходное функциональное назначение точек следующее:
1. лапароскоп,
2 и 3. эндодиссектор, эндоножницы, эндоклипер при работе на малой кривизне и на большой кривизне в теле желудка,
3. сшивающий аппарат для наложения гастроэнтероанастомоза,
4. второй эндобэбкокк для тракций желудка,
5. ретрактор для отведения печени.
В точки 6 и 7 можно вводить любой из указанных выше эндоинструментов, особенно в случаях неэффективного угла движения инструментами.
На каждый введенный в брюшную полость 12-мм троакар устанавливается конвертер SEALUP. Ценность этого конвертера в универсальности и в наличии двух каналов для пяти- и десятимиллиметровых инструментов. Для введения двенадцатимиллиметрового инструмента конвертер снимается.
После установки и фиксации троакаров производят тщательную ревизию брюшной полости, в ходе которой необходимо: идентифицировать язву или опухоль, размеры инфильтрата, наличие региональных метастазов, определить степень и характер пенетрации, определить уровень и границы резекции желудка. Отсутствие массивного спаечного процесса, пенетрации язвы, прорастания опухоли и регионального метастазирования позволяет решить вопрос о продолжении операции лапароскопическим путем.
Основные этапы лапароскопической резекции желудка по Бильрот-2 состоят в следующем:
1) мобилизация желудка по большой кривизне с пересечением большого сальника по бессосудистой зоне над поперечно-ободочной кишкой;
2) мобилизация желудка по малой кривизне;
3) пересечение сшивающим аппаратом двенадцатиперстной кишки и желудка;
4) наложение гастроэнтероанастомоза эндоскопическим сшивающим аппаратом;
5) закрытие отверстия в гастроэнтероанастомозе герниоклипером;
6) низведение и фиксация гастроэнтероанастомоза механическим швом в окне брыжейки поперечно-ободочной кишки.
Мобилизацию начинают с этапной эндокоагуляции и пересечения эндоножницами печеночно-желудочной связки для последующего свободного доступа к правой и левой желудочной артерии. По мере пересечения печеночно-желудочной связки постепенно обнажается сосуд, расположенный ближе к наружному контуру двенадцатиперстной кишки. При этом поэтапно выделяется холедох, из спаек выделяется желчный пузырь, постепенно выделяется двенадцатиперстная кишка (по типу мобилизации её по Кохеру). После рассечения печеночно-желудочной связки вверх и вниз до уровня правой и левой желудочной артерий производится изолированное выделение правой желудочной артерии. В большинстве случаев это легко удается выполнить эндодиссектором и эндоножницами. Правая желудочная артерия трижды клипируется в 1 - 1,5 см от стенки двенадцатиперстной кишки и пересекается между клипами. После этого желудок и двенадцатиперстная кишка по наружному контуру достаточно свободны, можно перейти к мобилизации желудка по большой кривизне. В случае резекции 1/2 желудка требуется мобилизация желудка на границе левой и правой желудочно-сальниковых артерий. Именно в этом бессосудистом месте по большой кривизне начинается мобилизация желудка. Для того, чтобы свободно подойти к правой желудочно-сальниковой артерии, рассекается эндоцожницами в бессосудистом месте желудочно-ободочная связка. После этого легко выделяется желудочно-сальниковая артерия и непосредственно у стенки желудка на уровне большой кривизны после двухкратного клипирования пересекается. Дальнейшая линия разреза представлена на рисунке штриховой линией. Мобилизация большого сальника производится строго вертикально к поперечно-ободочной кишке, при этом необходимо этапное клипирование.
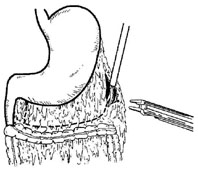 Рис.
3. Линия разреза и клипирования сосудов большого сальника.
Рис.
3. Линия разреза и клипирования сосудов большого сальника.
Опыт выполненных операций показывает, что при пересечении по представленной штриховой линии требуется два-три раза клипировать сосуды. В большинстве случаев они имеют типичное анатомическое строение. И лишь в некоторых случаях требуется дополнительное клипирование мелких сосудов. После вертикального пересечения сальника выявляется анатомическая бессосудистая зона у поперечно-ободочной кишки. Несколько сложнее происходит мобилизация желудка и двенадцатиперстной кишки на уровне препилорического отдела, так как в этой зоне имеется большее количество сосудов. Здесь приходится клипировать и пересекать сосуды – 3 - 4 сосуда. Особая осторожность требуется при выделении сосудов в непосредственной близости головки поджелудочной железы, у пилорического жома и луковицы двенадцатиперстной кишки. Затем приступают к мобилизации желудка по малой кривизне с клипированием и пересечением левой желудочной артерии. Чаще удается выделить левую желудочную артерию непосредственно у стенки желудка но малой кривизне. Изолированное выделение концевых ветвей левой желудочной артерии, их клипирование в 2 - 3 местах ведет к полной мобилизации малой кривизны желудка. Такого же успеха можно достичь благодаря однократному прошиванию аппаратом Endo GIA-30 с белой кассетой.
Для полной мобилизации желудка обычно требуется от 1 до 1,5 часов. Дальнейшие этапы лапароскопической резекции желудка складываются из обычных этапов, как и при выполнении открытой резекции желудка аппаратным методом. Важным моментом лапароскопической резекции желудка является умение работы со сшивающим аппаратом. До овладения лапароскопической резекцией желудка это умение хирург должен приобрести в открытой хирургии, т.к. сшивающие аппараты для открытых операций являются прототипом эндоскопических.
Мобилизованный желудок свободно смещается двумя эндобэбкокками вверх, к диафрагмальной поверхности печени. В зависимости от его размеров можно производить тракцию желудка в сторону пищевода или в сторону селезенки. При тракции желудка вверх хорошо обнажается мобилизованная двенадцатиперстная кишка. Обычно для пересечения мобилизованной двенадцатиперстной кишки требуется 2 аппликации аппарата Endo GIA-30 с синими кассетами. Прошивание и пересечение производятся но одной намеченной линии. Сшивающий аппарат накладывается на луковицу двенадцатиперстной кишки со стороны большой кривизны, после чего производится прошивание с пересечением. После первого прошивания кишки образуется угловая рана с наложенными трехрядными механическими швами. По этой же линии от угла раны, образованной механическими швами, второй раз накладывается Endo GIA-30 с синей кассетой, после чего второй раз прошивается и окончательно пересекается луковица двенадцатиперстной кишки. В результате образуется герметичная линия механического шва со стороны желудка и сформированная культя двенадцатиперстной кишки, после этого желудок легко поднимается и отводится вверх к пищеводу.
Намечается линия резекции желудка. Чаще всего эта линия идет от уровня мобилизации желудка, от уровня окончания правой желудочно-сальниковой артерии вверх к краю левой доли печени, на 3 - 4 см выше язвенного инфильтрата. Для полного пересечения желудка по предполагаемой линии резекции требуется 4 - 5 синих кассет.
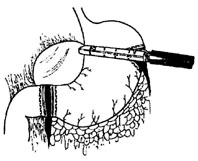 Рис.
4 Прошивание и пересечение желудка аппаратом
Endo GIA-30.
Рис.
4 Прошивание и пересечение желудка аппаратом
Endo GIA-30.
Прошивание и пересечение желудка аппаратом Endo GIA-30 с синими кассетами производится типично, как и при прошивании и пересечении двенадцатиперстной кишки. Можно для этой цели использовать аппарат Endo GIA-60 с синей кассетой, в этом случае для пересечения желудка достаточно 2 аппликации. Следует иметь в виду, что этот инструмент в диаметре 15 мм и, при отсутствии 15-мм троакара, можно временно удалить 12-мм троакар и в образовавшееся отверстие ввести аппарат Endo GIA-60 без троакара. Резецированный желудок лучше погружать в целлофановый мешочек, предварительно введенный в брюшную полость через один из троакаров.
Последняя манипуляция значительно облегчает конечный этап операции - извлечение желудка через небольшой разрез. Еще удобнее использовать специальный инструмент Endo Catch II, который раскрывается в виде "сачка" в брюшной полости, в него помещается удаляемый орган, затем инструмент закрывается, превращаясь в мешок.
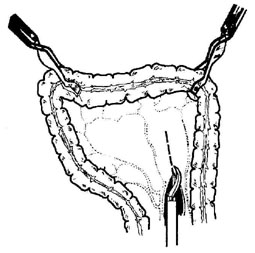 Рис.
5. Тракция
поперечно-ободочной кишки эндобэбкокками
и формирование окна в мезоколон.
Рис.
5. Тракция
поперечно-ободочной кишки эндобэбкокками
и формирование окна в мезоколон.
После пересечения желудка производится тракция поперечно-ободочной кишки для формирования окна в ее брыжейке. Для этого достаточно натянуть поперечно-ободочную кишку и мезоколон и эндоножницами с этапной эндокоагуляцией непосредственно произвести разрез вверх от трейцевой связки. Разрез производится длиной 4 - 5 см. Сразу после выполнения этого разреза эндобэбкокком берется тощая кишка приблизительно в 20 - 25 см от трейцевой связки и вводится в окно мезоколон. Второй эндобэбкокк в это время захватывает тощую кишку со стороны резецированного желудка, а поперечно-ободочная кишка опускается вниз. Таким образом, тощая кишка приближается к культе желудка и укладывается рядом.
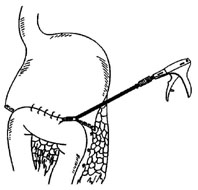 Рис.
6. Фиксация тонкой кишки к культе желудка
титановыми клипами апаратом для эндогерниопластики.
Рис.
6. Фиксация тонкой кишки к культе желудка
титановыми клипами апаратом для эндогерниопластики.
Принципиальным моментом является фиксация тощей кишки к культе желудка. Фиксация производится титановыми скобками аппаратом для герниопластики чуть выше (на 1 - 1,5 см) от ранее наложенной линии механического шва на желудке. Фиксация ручным швом в данной ситуации затруднительна. Естественно, что первый опыт работы с металлическими скобками, идущими вертикально в стенку кишки или желудка, вызывает справедливые сомнения у хирурга. Поэтому на рисунке представляем изученные нами особенности работы с аппаратом - эндогерниоклипером. Для надежной и неосложненной фиксации кишки и желудка между собой необходимо предварительно вывести бранши клипа из аппарата приблизительно на 3/4 его длины. Сначала прокалывается серозная оболочка желудка, а затем - серозная оболочка кишки. Благодаря этому аппарат не скользит по серозной оболочке, а кишка и желудок плотно соприкасаются друг с другом. После фиксации скобочным швом желудка и кишки в их стенках формируются расположенные в непосредственной близости друг от друга два отверстия в просвет желудка и тощей кишки для наложения гастро-энтероанастомоза аппаратом Endo GIA-30. Как правило, при рассечении стенок желудка и кишки пользуются эндодиссектором и эндоножницами, производя этапную коагуляцию всех слоев стенки желудка и кишки. После вскрытия просвета желудка и кишки производится эвакуация электроотсосом содержимого. Отверстия для последующего введения бранш сшивающего аппарата GIA-30 должны достигать 0,5 см. При наличии таких отверстий бранши сшивающего аппарата свободно проникают в просвет желудка и тощей кишки.
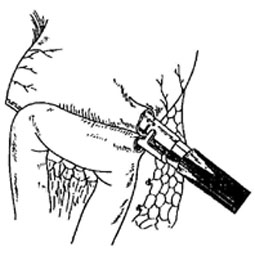 Рис.
7. Формирование гастроэнтероанастомоза аппаратом
Endo GIA-30.
Рис.
7. Формирование гастроэнтероанастомоза аппаратом
Endo GIA-30.
Аппарат Endo GIA-30 вводится в один из троакаров, расположенных в проекции левого латерального канала, как правило, через нижний троакар. Браншу аппарата с установленной синей кассетой вводят в желудок в первую очередь. Затем, после введения бранши в желудок, вторую металлическую браншу аппарата вводят в тощую кишку. В это же время производят тракцию стенок желудка и тощей кишки на аппарат для полного введения его бранш в просвет органов (до конца отметок на аппарате). После выполнения этих манипуляций аппарат свободно закрывается, снимается предохранитель и производится прошивание стенок желудка и кишки с одновременным рассечением и формированием трехрядного механического гастроэнтероанастомоза. После извлечения Endo GIA-30 из просвета желудка и кишки необходимо осмотреть анастомоз. Лапароскоп подводится непосредственно к просвету желудка и тощей кишки, в результате чего хорошо виден наложенный анастомоз. Этот момент важен для оценки его состояния, включая полноту прошивания и рассечения тканей, наличие кровотечения из линии анастомоза. Убедившись, что анастомоз сформирован без видимых осложнений, можно приступать к дальнейшему этапу операции - закрытию отверстия в анастомозе. Для этого требуется сшивание стенки желудка и тощей кишки. В ряде зарубежных работ имеются указания на закрытие этого окна аппаратом Endo GIA-30. Мы избегаем этой методики, т.к. убедились, что при использовании для формирования анастомоза аппарата Endo GIA-30 второе прошивание и закрытие окна анастомоза значительно суживает его просвет. В этой ситуации вновь используется эндогерниоклипер, закрывая окно в анастомозе однорядным или двухрядным механическим швом с использованием титановых скобок.
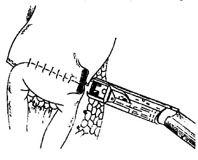 Рис.
8. Формирование гастроэнтероанастомоза герниоклиппером.
Рис.
8. Формирование гастроэнтероанастомоза герниоклиппером.
Достаточно эндогерниоклипер привести в рабочее положение и ввести в брюшную полость и произвести прошивание скобками. Во время наложения скобок на стенки кишки и желудка необходима одновременная тракция желудка и кишки для их сближения. Этим достигается полное закрытие просвета анастомоза. В зависимости от индивидуальных особенностей и качества наложенного шва требуется наложение однорядного или двухрядного механического шва. Для закрытия отверстия в анастомозе можно также использовать ручной аппаратный шов (одно- или двухрядный) инструментом Endo-Stich с использованием шовного материала Polysorb 2/0. После закрытия остается последний этап - низведение анастомоза в окно мезоколон и фиксация его. Низведение анастомоза в окно мезоколон производится эндобэбкокком. Производим тракцию за тощую кишку с одновременной подачей желудка через окно мезоколон эндобэбкокком. Фиксация желудка в окне мезоколон к краям окна в мезоколон вновь производится эндогерниоклипером. Клипируем края раны мезоколон к серозной оболочке желудка выше сформированного анастомоза. После фиксации анастомоза необходимо промыть и осушить брюшную полость. Чаще всего необходимо выполнить дренирование брюшной полости через рану на месте троакара из левого подреберья - рана расширяется до 3 - 4 см. Крючками раздвигаются мышцы передней брюшной стенки, раскрывается шире брюшина, и такой раны достаточно для извлечения резецированного желудка даже с большим язвенным инфильтратом. Брюшная полость повторно осматривается, контролируется установка дренажа. Повторно можно произвести эвакуацию крови и скопившейся в брюшной полости жидкости.
В течение первых дней послеоперационного периода мы не можем указать на какие-либо отрицательные моменты. Среди явных преимуществ течения послеоперационного периода проявились: ранняя физическая активизация больного, ранняя функциональная активность работы желудочно-кишечного тракта, отсутствие выраженных воспалительных проявлений со стороны гастроэнтероанастомоза.
Несмотря на значительную длительность лапароскопической резекции желудка (от 2 до 6 часов) уже по истечении постнаркозного периода больной способен подниматься и обслуживать себя. Тем не менее, как правило, все пациенты предъявляют жалобы на боль в животе, локализующуюся в эпигастрии и подпеченочном пространстве. Несмотря на наличие 5 - 6 ран после проколов передней брюшной стенки, к первым суткам лечения местная боль сохраняется только в ране, через которую извлекаем желудок.
Первые сутки послеоперационного периода у всех пациентов наблюдается температурная реакция. Колебания ее достигали больших показателей от 37,2 до 39. После плановых лапароскопических резекции желудка пик температуры приходится на 3-й сутки и потом она 2 - 3-е суток держится на субфебрильных цифрах, постепенно снижаясь до нормы.
Несмотря на наличие температурной реакции, в анализах крови отмечались незначительные изменения, характерные для воспалительного процесса.
Длительность болевого синдрома и температурной реакции в целом совпадали и постепенно исчезали к 3 - 4-му дню послеоперационного периода.
У всех оперированных нами пациентов отмечена активная перистальтика кишечника уже к концу первых суток послеоперационного периода. Этот срок характеризовался началом отхождения газов, а к концу 2-х суток наличием стула. Это также мы можем связать с малотравматичностью доступа и самой резекции желудка. Начало кормления наших пациентов связано с началом активной функции кишечника, т.е. обычно к середине 2-го послеоперационного дня. Расширение диеты в последующие дни не несет больному каких-либо неприятных ощущений при соблюдении традиционных рекомендаций. Так же как в открытой хирургии, в основе этих рекомендаций лежит дробное до 6 - 7 раз питание с соблюдением относительно стандартного набора пищевых продуктов. Эти же рекомендации оставались актуальными для больного после выписки его из стационара. Таким образом, налицо значительно более ранняя активизация больных, восстановление пищеварительной функции желудочно-кишечного тракта по сравнению с традиционными методами резекции желудка.
Гастродуоденоскония, выполненная контрольно у всех пациентов на 4-е и 7-е сутки послеоперационного периода, свидетельствует о благоприятном течении процесса заживления анастомоза. Гастроэнтероанастомоз лапароскопической резекции желудка отличает стандартность размера. Его размер достигает 2,5 см, в первые сутки он "зияет". Уже с 4-х суток не отмечается выраженной гиперемии слизистой анастомоза, десквамации слизистой в области анастомоза. В этот срок появляется хорошо заметная перистальтика в зоне анастомоза.
Во время контрольной гастродуо-деносконии к 7-м суткам "зияние" анастомоза постепенно исчезает. Линия анастомоза вместе со стенкой желудка и кишечника перистальтирует. В момент перистальтики открывается просвет кишки на различных участках по всей длине анастомоза.
Опыт лапароскопических резекций в мире пока невелик, поэтому мы подробно остановились на ближайшем послеоперационном периоде. Хотелось бы сослаться и на сводные данные интернационального клуба желудочной хирургии. Он включает 117 операций, в том числе гастрэктомий, у пациентов в возрасте 24 - 91 год (средний возраст 49 лет). У 34,6% показанием к операции был рак желудка. Длительность операции колебалась в пределах 90 - 360 мин. (в среднем - 210 мин.), конверсия составила 5%, длительность госпиталь ного периода - 8 дней, восстановление нормального образа жизни - 17,4 дня, смертность - 2,5%.
Обращает на себя внимание сообщение Р. Hermanek, Сh. Wittekind (1994), которые при выполнении 10 субтотальных резекций и 15 гастрэктомий при злокачественных опухолях производили расширенную лимфаденэктомию.
Первый опыт операций, накопленный в мире, дает право говорить о возможности их лапароскопического выполнения, о наличии альтернативных вариантов в желудочной хирургии.
По всей вероятности только накопление количественного и качественного опыта, солидных экспериментальных данных, а также анализ достаточного числа отдаленных результатов даст право хирургам судить о преимуществах и недостатках операций, лапароскопических технологий в желудочной хирургии.